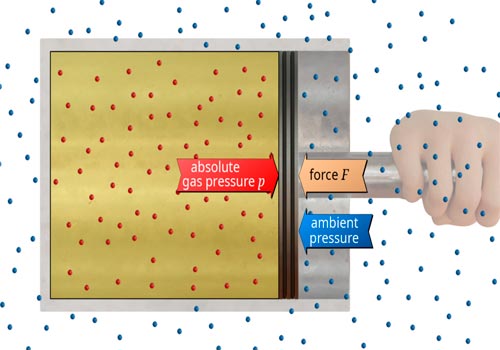
Средняя длина свободного пути
Тепловое движение молекул газа сопровождается не только ударами молекул о стенки сосуда, в котором заключен газ, но и их взаимными столкновениями.
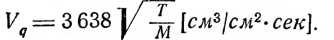

Между средней длиной свободного пути (X) и средним числом столкновений молекулы в 1 сек (z) существует определенное соотношение. Легко сообразить, что Х= -р т. е. при неизменной температуре газа (pa = const) средняя длина свободного пути обратно пропорциональна среднему числу столкновений молекулы в 1 сек.
Кинетическая теория показывает, что средняя длина свободного пути молекул X обратно пропорциональна молекулярной концентрации газа N следовательно, при неизменной температуре средняя длина свободного пути молекул обратно ппопоопиональна давлению газа:
Представляет собой, вообще говоря, пространственную ломаную линию, прямолинейные участки которой соответствуют свободному передвижению молекулы (без столкновений) (рис. 3-1); точки, где молекула меняет свое направление, соответствуют моментам столкновения данной молекулы с какой-либо другой. Поскольку тепловое движение беспорядочно, прямолинейные пути молекул между двумя столкновениями не могут быть одинаковыми; тем не менее благодаря существованию определенного закона их распределения мы и здесь можем аналогично понятию о средней скорости теплового движения ввести понятие о среднем расстоянии, проходимом молекулами между дву
или
где k — постоянный коэффициент, зависящий только от рода газа и температуры.
Для средней длины свободного пути имеет место выражение
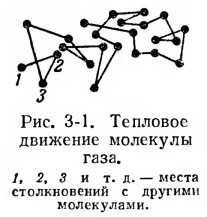



где Nj — молекулярная концентрация газа;
о -диаметр молекулы;
Т — абсолютная температура газа;
С — постоянная, зависящая от рода газа.
В является экспериментальной поправкой, показывающей, что Я зависит от температуры газа (прямая зависимость).
Если через Я273 обозначить среднюю длину свободного пути при 0° С, а через Яг при Т° абс., то нетрудно подсчитать. что
Таблица 3-1
|
Газ |
X, см, при 0° С и 760 мм рт. ст |
С |
|
n2 |
5,99-10-6 |
102,7 |
|
Аг |
6,35-10-6 |
147,8 |
|
н2 |
11,23-10-6 |
82,8 |
|
о2 |
6,47-10-6 |
136 |
|
Воздух |
6,08-10-6 |
124 |
Для представления о величине К при различных давлениях целесообразно рассмотреть табл. 3-2, где в качестве примера указаны длины свободного пути молекул воздуха при различных давлениях и температуре 20° С.
По формуле (3-3)
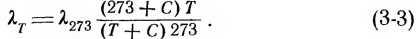
По формуле (3-3) можно определять длины свободных путей молекул газа при данной температуре, если длина свободного пути известна для другой температуры.
Примеры вычисленных значений X приведены в табл. 3-1.

На основании формулы (3-1) и по данным табл. 3-2 для воздуха при 20° С можно определить произведение длины свободного пути молекулы и давления:
Пользуясь этим соотношением, можно легко подсчитать значение Z для воздуха при любом давлении, выраженном в мм рт. ст